مطالبی در مورد کرومیک اسید:
اسید کرومیک چیست؟
کروم یکی از عناصر جدول تناوبی می باشد که از نشان Cr و عدد اتمی ۲۴ برخوردار می باشد.
کروم یا کرومیوم فلزی سخت، براق و به رنگ خاکستری فلزی با جلا پذیری بالا و نقطه جوش بالا و مقاومت
قابل توجه در برابر زنگزدگی و تیرگی می باشد. اکسید کرومیوم از بیش از ۲ هزار سال پیش در امپراتوری
چین برای روکش سلاحهای فلزی به کار برده می شد. کروم به عنوان یک عنصر در سال ۱۷۶۱ کشف شد
و نخست به عنوان رنگدانه استفاده می شد. در ۱۷۹۷ فلز کروم برای اولین بار از سنگ معدنی آن جدا شد.
از آن زمان تاکنون تقریباً تمام کروم دنیا از سنگ معدنی کرومیت به دست میآید. ارزش این فلز بیشتر به
دلیل مقاومت بسیاربالای آن در برابر زنگ زدگی و فرسایش می باشد. به خصوص زمانی کشف شد
که افزودن کروم به فولاد تأثیر قابل توجهی در جلوگیری از فرسایش و تیرگی فولاد دارد.اکنون حدود ۸۵ درصد
مصرف کروم دنیا برای ساخت فولاد ضدزنگ (که حداقل ۱۰.۵ درصد حجم آن را کروم متشکل می شود و همینطور آبکاری با کروم می باشد.
کروم به شکل سنگ معدن کرومیت ( H2CrO4 ) استخراج می شود. این عنصر را بصورت تجاری با حرارت دادن
این سنگ معدن در حضور آلومینیوم یا سلیکون تهیه می کنند. تقریبا نیمی از سنگ معدن کرومیت جهان در
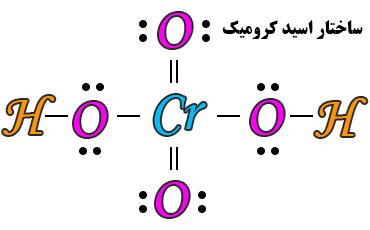
آفریقای جنوبی تولید می شود. اسید کرومیک دارای ساختار فرضی H2CrO4 است. جالب است بدانید
که نه اسید کرومیک و نه اسید دی کرومیک در طبیعت یافت نمی شوند اما آنیونهای آنها در ترکیبات متنوعی یافت می شود.
تری اکسید کروم CrO3 (اسید بدون آب اسید کرومیک) بصورت تجاری، بعنوان اسید کرومیک بفروش می رسد.
نام های دیگر اسید کرومیک (H2CrO4) شامل کرومیک اسید. Chromic(VI) acid ،Tetraoxochromic acid می باشد.
اسید کرومیک از نظر خواص شباهت زیادی به اسید سولفوریک دارد و هردو جزء اسیدهای قوی دسته بندی می شوند.
این ماده به دلیل توانایی “براق کردن” بطور گسترده ای در صنعت تعمیر ابزار و وسایل مورد استفاده قرار می گیرد
اما به دلیل نگرانی های بهداشتی و زیست محیطی ، بسیاری از افراد استفاده از
این ماده شیمیایی را در تعمیرگاه های خود متوقف کرده اند. اسید کرومیک بیشتر به صورت محلول آبی ۱۰٪ در دسترس است.
تاریخچه کشف اسیدکرومیک
اولین بار جان ری طبیعت شناس انگلیسی در سال 1671 این اسید را از تقطیر توده ای از مورچه های مرده جدا کرد.
اما سنتز شیمیایی آن اولین بار توسط شیمیدان فرانسوی ژوزف گیلوساک از اسید هیدروسیانیک انجام گرفت.
در سال 1855 شیمیدان فرانسوی دیگری به نام Marcellin berthelot اسید فرمیک را با استفاده
از مونو اکسید کربن سنتز کرد ، شبیه روشی که امروزه مورد استفاده قرار می گیرد.
کاربرد اسیدکرومیک (Chromic Acid)
اسید کرومیک جهت آبکاری کرم در صنعت آبکاری مورد استفاده قرار می گیرد
و در واکنش با آنود کرم باعث درخشندگی و براق نمودن فلز آبکاری شده می گردد.
البته اخیرا بجای آبکاری از اسپری رنگ کروم نیز استفاده می شود.
در آزمایشگاه ها برای تمیز کردن حمامها استفاده می شود تا باقیمانده مواد آلی را از وسایل شیشه ای پاک کند .
این ماده همچنین برای حکاکی ، قلم زنی و برنزه کردن مورد استفاده قرار می گیرد.
از این ترکیب خورنده برای رنگ آمیزی چوب ، استخوان و عاج سیاه نیز استفاده می شود.
در شیمی آلی ، از محلول های رقیق اسید کرومیک برای اکسیداسیون الکلهای اولیه یا ثانویه جهت
سنتز آلدهیدها و کتونهای مربوطه استفاده می شود ولی گروه های الکل سوم تحت تاثیر این ماده قرار نمی گیرند.
از آنجاییکه اکسیداسیون با تغییر رنگ ترکیب از نارنجی به سبز- آبی نشان داده می شود ،
همچنین به عنوان تست تحلیل کیفی برای حضور الکل های اولیه یا ثانویه کاربرد دارد.
برند های اسیدکرومیک در بازار
در بازار برند های متفاوتی از کشور های چین، هند، المان، قزاقستان، ترکیه ، ایتالیا و آلمان به فروش می رسد،
معمولا بشکه های آنها 50 کیلویی و در بعضی موارد 25 کیلویی هستند، برند چینی در بشکه های سرمه ای رنگ،
برند ترکیه در بشکه های آبی رنگ و برند ویشنو هند در بشکه سبز رنگ به فروش می رسند.

خطرات استفاده از کروم و موارد ایمنی

تماس با این ماده به عنوان یک ماده اکسید کننده قوی که برای تمیز کردن فلزات مختلف مورد استفاده قرار می گیرد،
باعث انعقاد پروتئین های بدن می شود. دوز کشنده برای این ماده بین ۵ تا ۱۰ گرم است که منجر به مشکلات
گوارشی و به دنبال آن سرگیجه ، گرفتگی عضلات ، گرفتگی عروق محیطی و کما می شود.شستشوی معده
با آب اولین خط درمان هنگام بلع این ماده شیمیایی است ولی شستشو با محلول هیپوسولفیت سدیم
و سپس محلول بافر فسفات پادزهر ویژه اسید کرومیک است.
اثرات سمی:
تماس پوستی با گروهی از ترکیبات کروم موجب زخم در پوست میشود. در افراد دارای حساسیت،
واکنشهای حساسیتی میتواند شامل قرمزی شدید پوست و تورم باشد.
زخمهای پوستی، واکنشهای خورنده روی تیغه بینی و درماتیتهای تحریکی از جمله دیگر عوارضی است
که در افراد در معرض کروم شش ظرفیتی گزارش شده است. زخم و سوراخ شدن تیغه بینی در دو سوم افرادی
که در معرض این ماده بصورت اسید کرومیک در تراکمهای بیش از 20 میکروگرم بر متر مکعب بودهاند، مشاهده شده است.
بررسی کارگرانی که بصورت شغلی در معرض استنشاق کروم بودهاند نشان داده است
که استنشاق کروم شش ظرفیتی با تحریک دستگاه تنفس موجب تحریک راههای هوایی ریه و انسداد آنها میگردد.
تحریک طولانی مدت ریهها در نتیجه استنشاق ذرات این ماده ممکن است تحریک مزمن و احتقان (پرخونی غیر عادی)،
حساس شدن ریهها و در نتیجه ظهور علایم آسم و گروهی از دیگر اختلالات ریوی را در پی داشته باشد.
البته موضوع سرطانزایی ترکیبات کروم شش ظرفیتی و افزایش ابتلای به سرطان ریه بواسطه مواجهه مزمن امری مسلم و اثبات شده است.
بررسی کارگرانی که با کروم شش ظرفیتی، بویژه در تراکمهای بیش از 20 میکروگرم بر متر مکعب مواجهه داشتهاند، نشان داده است
که این عده دچار اختلالاتی در کلیهها بویژه از نوع توبولی شدهاند. مواجهه با ترکیبات کروم شش ظرفیتی با اختلالاتی در کبد نیز همراه است.
گزارش مربوط به یک بررسی در میان آبکاران در معرض اسید کرومیک نشان داده است
که مواجهه طولانی مدت با مقادیر اندکی از کروم با اختلالات خفیف تا متوسط کبدی ظاهر گشته است.
ابتلاء به اختلالات سیستم ایمنی در بدن نیز بواسطه مواجهه مزمن با ترکیبات کروم شش ظرفیتی گزارش شده است.
ورود ترکیبات کروم از راه گوارش بویژه خوردن مقادیر زیادی از ترکیبات کروم شش ظرفیتی (مواجهه حاد) میتواند موجب
ناراحتی و زخم معده شده و در ادامه تشنج، آسیب به کبد و کلیهها و حتی مرگ را در پی داشته باشد.
روش صحیح نگهداری
این ماده در محیط خشک، تاریک و دارای تهویه مناسب نگهداری شود.اتاق انبار ضد حریق باشد.فقط در ظرف اصلی نگهداری شود
و روی ظروف باید به نحو صحیح برچسب گذاری شود . دور از چوب و کاغذ و سایر مواد احیاءکننده (آتش گیر) نگه داشته شود.
ظرفهای خالی اسید کرمیک اگر به عنوان ظروف نگهداری ضایعات مورد استفاده قرار گیرد میتواند منجر به آتش سوزی شود.
بنابراین هیچگاه نباید بدین منظور از آن استفاده نمود.ظرف های اسید کرمیک، مانند تمام مواد شیمیایی دیگر،
حتی وقتی که مورد استفاده قرار نمی گیرند، باید کاملا بسته و محفوظ باشند.
محصولات ناسازگار:
اكسيد كنندههای قوی. عوامل احيا كننده قوی. فلزات. مواد قابل احتراق. آلومينيوم

